我院消化內(nèi)科陳微微博士在《Molecular Cancer》期刊發(fā)表重要研究論文

近日,,我院消化內(nèi)科陳微微博士在《Molecular Cancer》(中科院1區(qū),、Top期刊,IF=27.7)期刊發(fā)表了題為“miR-483-5p-mediated activating of IGF2/H19 enhancer up-regulates IGF2/H19 expression via chromatin loops to promote the malignant progression of hepatocellular carcinoma”的重要研究論文,,陳微微博士是該論文共同第一作者(排名第一),。

原發(fā)性肝細胞癌(HCC)是全球癌癥相關(guān)死亡的第二位致死原因,我國HCC死亡人數(shù)約占全球肝癌死亡人數(shù)的一半,。HCC惡性程度高,,病死率高,預后差,。近十年來,,雖然HCC在手術(shù)、化療藥物等治療方法上取得一定進展,,但其預后仍然無明顯改善,。因此,探索HCC發(fā)生發(fā)展機制,,挖掘新的信號通路分子靶點,,以期開發(fā)新的靶向藥物至關(guān)重要。近年來,,該團隊和其他學者研究表明,,IGF2 基因在多種惡性腫瘤包括HCC中的表達水平明顯增高,且主要以P3 mRNA和P4 mRNA高表達為主,,尤其是P3 mRNA 的上調(diào)最為顯著,。IGF2促進HCC侵襲與轉(zhuǎn)移,高表達IGF2的HCC患者預后較差,。另一方面,,研究顯示H19基因在多種惡性腫瘤包括HCC中的表達水平也明顯增高,H19 RNA促進肝癌細胞增殖,、遷移和侵襲,。但是,HCC中IGF2和H19基因過表達的機制尚未完全明確,。
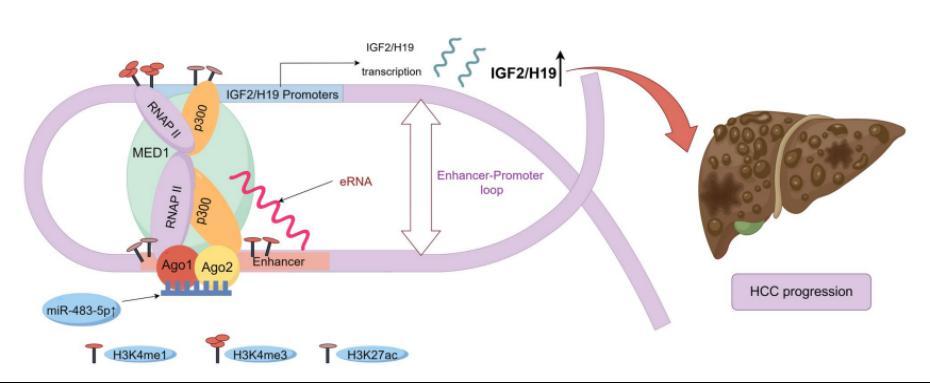
該研究成功驗證了miR-483-5p通過靶向IGF2/H19增強子上調(diào)肝癌細胞IGF2和H19的表達,,并闡明了其具體分子機制。具有以下創(chuàng)新點:(1)增強子RNA(eRNA)按照長度劃分大多屬于lncRNA,,但其不是普通lncRNA,。該研究將普通lncRNA調(diào)控基因表達機制的重要方式之一,,即形成lncRNA-protein-目標基因啟動子復合物。這種調(diào)控方式引入到該研究中,,推測在該研究中IGF2/H19 eRNA很可能與MED1結(jié)合成IGF2/H19 eRNA-MED1復合物,,后者再靶向遠隔的IGF2和H19基因啟動子,形成IGF2/H19 eRNA-MED1-IGF2/H19啟動子復合物,,進而激活I(lǐng)GF2和H19基因表達,。(2)近年來,miRNA調(diào)控機制的重要進展之一是在轉(zhuǎn)錄水平促進基因表達,,既往研究表明miRNA可以靶向增強子促進基因表達,,這是一種新的調(diào)控方式,但其調(diào)控機制尚未被探索,,該研究率先對此進行探索性研究,,闡明了其具體分子機制,結(jié)果有助于對miR-483-5p調(diào)控基因表達機制的認識提高到一個新高度,,豐富miRNA調(diào)控機制內(nèi)容,,同時為肝癌靶向治療提供新思路和靶標奠定理論基礎。
該研究得到了國家自然科學基金項目,、貴州省科技廳基礎研究計劃項目等經(jīng)費資助,。
專家介紹

陳微微 中共黨員 醫(yī)學博士
碩士研究生導師 遵義醫(yī)科大學博士后(入站)
副主任醫(yī)師 消化內(nèi)科副主任
貴州省高層次創(chuàng)新型“千層次”人才
遵義醫(yī)科大學“臨床名醫(yī)”人才
國家衛(wèi)生健康委“十·四五”規(guī)劃教材編委
曾獲國家實用新型專利 3 項,參編學術(shù)專著/教材 3 部,,開展新技術(shù)/新項目 5 項,。主持及參與國家級科研項目 1 項、省部級科研項目 1 項,、市廳級科研項目 3 項,。在國內(nèi)/外著名期刊發(fā)表各類學術(shù)論文 24 篇,其中SCI論文影響因子累計達70分,,單篇最高影響因子 27.7 分,。
擅長:消化系統(tǒng)疾病的診治、胃/腸鏡檢查及內(nèi)鏡下微創(chuàng)治療,,尤其是超聲內(nèi)鏡下手術(shù)及胃腸道腫瘤等相關(guān)疾病的診治,。
門診時間:每周三(全天)· 遵義市第一人民醫(yī)院鳳凰院區(qū)門診
圖文丨科研部
一審丨謝杰
二審丨屠琳
三審丨羅勇
掃一掃 手機端瀏覽

